2024年9月13日,1929cc威尼斯谢金兵教授团队,在国际知名学术期刊《Advanced Materials》在线发表了题为“Open-Source Throttling of CD8+ T Cells in Brain with Low-Intensity Focused Ultrasound-Guided Sequential Delivery of CXCL10, IL-2, and aPD-L1 for Glioblastoma Immunotherapy”的研究论文,报道了一种关于CD8+ T细胞的“开源节流”策略,能够有效提升胶质母细胞瘤的免疫治疗疗效,并通过激活长效的免疫记忆预防肿瘤复发。
胶质母细胞瘤(glioblastoma,GBM),一种极具侵袭性的脑肿瘤。尽管手术、放疗和化疗等传统治疗手段在一定程度上延长了患者生存期,但GBM的复发率仍然很高、预后较差。近年来,免疫治疗被认为是肿瘤治疗的前沿领域,尤其是抗PD-1/PD-L1等免疫检查点抑制剂在多种癌症中显示了显著疗效。然而,GBM的免疫治疗效果不佳,主要原因在于其免疫抑制性肿瘤微环境(tumor microenvironment,TME),导致CD8+ T细胞浸润不足且容易耗竭。此外,血脑屏障(blood-brain barrier,BBB)也严重阻碍了大分子免疫治疗药物的有效递送。因此,如何突破BBB,增强T细胞在肿瘤中的浸润并恢复其功能,成为GBM免疫治疗中的关键挑战。
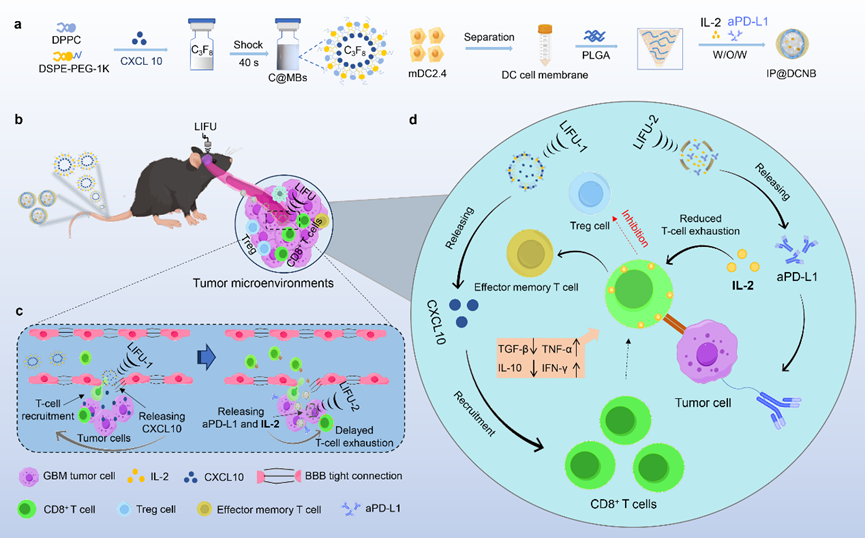
本研究通过低强度聚焦超声(low-intensity focused ultrasound,LIFU)引导CXCL10、IL-2和PD-L1抑制剂的序贯递送,实现GBM区域的CD8+ T细胞的“开源节流”效应。将CXCL10加载到微泡上,利用LIFU打开BBB并释放CXCL10以招募CD8+ T细胞。然后,利用LIFU引导将IL-2和aPD-L1递送到GBM区域,减轻CD8+ T细胞的耗竭并增强其抗肿瘤活性。实验使用了包括体内小鼠模型和体外细胞实验的综合方法来评估这种组合疗法的有效性。该策略为GBM的免疫治疗提供了新的思路,具有广泛的临床应用潜力。
1929cc威尼斯2022级博士研究生董磊为本文第一作者。1929cc威尼斯谢金兵教授、居胜红教授、张海军教授、陈小元教授为本文共同通讯作者。该研究得到国家自然科学基金、国家重点研发计划、东南大学博士生创新能力提升计划等项目资助。
论文链接:https://onlinelibrary.wiley.com/doi/full/10.1002/adma.202407235
 搜索
搜索