2024年10月30日,1929cc威尼斯、发育与疾病相关基因教育部重点实验室陶艳梅教授团队在国际权威综合性杂志《PNAS》在线发表题为Pan-ErbB inhibition impairs cognition via disrupting myelination and aerobic glycolysis in oligodendrocytes的研究论文。

青春期是中枢神经系统发育成熟的关键时期,少突胶质细胞产生的髓鞘是青春期大脑发育中最活跃的成分之一,这使得中枢髓鞘成为诸如精神分裂症等通常在青春期发病的精神疾病的易感目标。随着影像学技术的发展,越来越多的研究指出白质异常是精神分裂症的一个新兴特征,但其潜在的病理生理机制尚不为人所知。白质是髓鞘聚集的区域,少突胶质细胞的膜结构包绕在神经元轴突后特化形成的髓鞘对神经元的动作电位传导至关重要。近年的研究还发现,少突胶质细胞可以通过髓鞘向轴突传递乳酸等物质,为轴突能量代谢提供底物,但其中的调控机制并不清楚。
酪氨酸激酶受体ERBB4及其配体neuregulin 1 (NRG1) 在不同人群的精神分裂症患者中出现异常表达和与精神分裂症相关的遗传多态性。NRG/ErbB信号通路已被证明对外周神经系统的髓鞘化至关重要,但在中枢髓鞘发育中的作用尚有争议, ErbB信号通路与精神分裂症白质病理特征之间的关系及其深层机制也尚未可知。
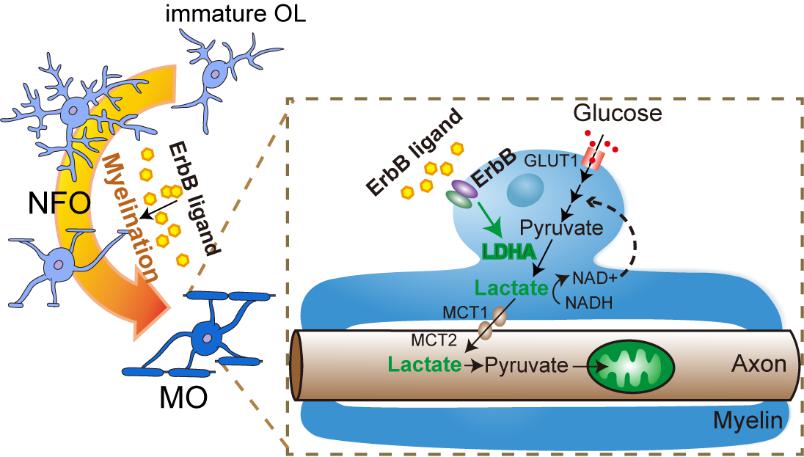
研究团队利用遗传工程小鼠实现在小鼠青少年时期分别特异性靶向少突胶质前体细胞(OPC)、新生成少突胶质细胞(NFO)或成熟少突胶质细胞(MO),在细胞内广谱抑制ErbB信号通路,以探究ErbB信号通路通过髓鞘机制影响精神分裂症病理病症的可能性。该研究结合大量在体和离体实验分析,明确了ErbB信号通路对髓鞘发育的重要作用和细胞机制。同时,研究团队意外发现 MO中的ErbB信号通路并不影响髓鞘发育,但通过影响K-Ras活性调控MO表达乳酸脱氢酶A(LDHA),从而影响MO通过有氧糖分解(Aerobic glycolysis)供给轴突能量底物的生理过程(如下图所示)。特异性抑制MO中的ErbB信号通路导致能量应激下的轴突传导功能下降。有趣的是,髓鞘结构缺陷会导致小鼠工作记忆缺陷,而当髓鞘结构完整但有氧糖分解途径受损时也会导致小鼠工作记忆缺陷。这些发现强调了ErbB信号通路在白质完整性和功能中不可或缺的作用,并为白质异常造成认知障碍的机制提供了多维度见解。
该研究的第一作者为陶艳梅教授和西湖大学贾洁敏教授合作指导的浙江大学-西湖大学联合培养博士生胡旭,通讯作者陶艳梅教授指导的东南大学和杭州师范大学研究生为其他主要参与者。杭州师范大学邱猛生教授和浙江大学沈颖教授提供相关技术支持。该研究得到国家自然科学基金、“脑科学与类脑研究”国家科技重大专项、东南大学新进教师人才引进启动经费等项目资助。
论文链接:https://www.pnas.org/doi/full/10.1073/pnas.2405152121
 搜索
搜索